Đăng nhập
Thuốc Lucirip Ripretinib là thuốc gì
Thuốc Lucirip Ripretinib là một chất ức chế kinase được sử dụng để điều trị khối u mô đệm đường tiêu hóa tiến triển (GIST) không đáp ứng đầy đủ với các chất ức chế kinase khác như sunitinib và imatinib.Đây là loại thuốc đầu tiên được phê duyệt như một liệu pháp bậc bốn trong bối cảnh cụ thể của điều trị trước đó với tối thiểu 3 chất ức chế kinase khác
Chỉ định của thuốc Lucirip Ripretinib
Qinlock là một chất ức chế kinase được chỉ định để điều trị cho bệnh nhân trưởng thành bị khối u mô đệm đường tiêu hóa tiến triển (GIST) đã được điều trị trước đó với 3 hoặc nhiều thuốc ức chế kinase, bao gồm cả imatinib.Dược lực học của thuốc Lucirip Ripretinib
Là một chất ức chế kinase phổ rộng, ripretinib ức chế các đột biến gen khác nhau, tăng tỷ lệ sống sót không tiến triển ở bệnh nhân có khối u mô đệm đường tiêu hóa tiến triển (GIST). Nó có hiệu quả trong điều trị các đột biến kháng hóa trị với các chất ức chế kinase khác, chẳng hạn như imatinib.Ripretinib có xu hướng gây rối loạn chức năng tim và bệnh ác tính da nguyên phát mới. Điều quan trọng là phải đo phân suất tống máu tim trước và trong khi điều trị cũng như thực hiện các đánh giá da liễu thường xuyên.
Cơ chế hoạt động của thuốc Lucirip Ripretinib
Protein kinase đóng vai trò quan trọng trong chức năng tế bào và rối loạn điều hòa của chúng có thể dẫn đến ung thư. Ripretinib ức chế protein kinase bao gồm thụ thể yếu tố tăng trưởng A (PDGFRA) và KIT có nguồn gốc từ tiểu cầu đột biến và loại hoang dã gây ra phần lớn khối u mô đệm đường tiêu hóa (GIST). Trong ống nghiệm, ripretinib đã được chứng minh là ức chế các gen PDGFRB, BRAF, VEGF và TIE2.Ripretinib liên kết với các thụ thể KIT và PDGFRA có đột biến trên các exon 9, 11, 13, 14, 17 và 18 (đối với đột biến KIT) và exon 12, 14 và 18 (đối với đột biến PDGFRA). "Túi chuyển đổi" của protein kinase thường liên kết với vòng kích hoạt, hoạt động như một "công tắc bật-tắt" của kinase. Ripretinib tự hào có cơ chế hoạt động kép độc đáo liên kết với túi chuyển đổi kinase cũng như vòng kích hoạt, do đó tắt kinase và khả năng gây ra sự phát triển tế bào rối loạn điều hòa của nó.
Hấp thụ
Ripretinib được hấp thu trong đường tiêu hóa và đạt được Tmax trong 4 giờ, với nồng độ ở trạng thái ổn định đạt được trong vòng 14 ngày.Thể tích phân bố
Thể tích phân bố trung bình của ripretinib là 307 L.Liên kết protein
Ripretinib liên kết hơn 99% với albumin và glycoprotein axit alpha-1.Trao đổi chất
Ripretinib được chuyển hóa bởi phân họ enzym CYP3A với sự đóng góp từ CYP2D6 và CYP2E1 vào chất chuyển hóa hoạt động của nó, DP-5439.Tác dụng phụ của thuốc Lucirip Ripretinib
Hội chứng rối loạn hồng cầu lòng bàn tay-bàn chân (PPES): Trong INVICTUS, PPES Cấp độ 1–2 xảy ra ở 21% trong số 85 bệnh nhân nhận Qinlock. PPES dẫn đến ngừng liều ở 1,2% bệnh nhân, gián đoạn liều ở 2,4% bệnh nhân và giảm liều ở 1,2% bệnh nhân. Dựa trên mức độ nghiêm trọng, giữ lại Qinlock và sau đó tiếp tục ở cùng một hoặc giảm liều.Bệnh ác tính da nguyên phát mới: Trong INVICTUS, ung thư biểu mô tế bào vảy da (cuSCC) xảy ra ở 4,7% trong số 85 bệnh nhân được điều trị Qinlock với thời gian trung bình là 4,6 tháng (khoảng 3,8 đến 6 tháng). Trong quần thể an toàn gộp lại, cuSCC và keratoacanthoma xảy ra lần lượt ở 7% và 1,9% bệnh nhân. Ở INVICTUS, khối u ác tính xảy ra ở 2,4% trong số 85 bệnh nhân được điều trị Qinlock. Trong nhóm dân số an toàn gộp lại, khối u ác tính xảy ra ở 0,9% bệnh nhân. Thực hiện đánh giá da liễu khi bắt đầu Qinlock và thường xuyên trong quá trình điều trị. Kiểm soát các tổn thương da nghi ngờ bằng cách cắt bỏ và đánh giá bệnh lý da liễu. Tiếp tục Qinlock với liều lượng tương tự.
Tăng huyết áp: Trong INVICTUS, tăng huyết áp độ 1-3 xảy ra ở 14% trong số 85 bệnh nhân được điều trị Qinlock, bao gồm cả tăng huyết áp độ 3 ở 7% bệnh nhân. Không bắt đầu Qinlock ở bệnh nhân tăng huyết áp không kiểm soát. Theo dõi huyết áp theo chỉ định lâm sàng. Dựa trên mức độ nghiêm trọng, giữ lại Qinlock và sau đó tiếp tục ở cùng một hoặc giảm liều hoặc ngừng vĩnh viễn.
Rối loạn chức năng tim: Trong INVICTUS, suy tim xảy ra ở 1,2% trong số 85 bệnh nhân được điều trị Qinlock. Trong nhóm dân số an toàn gộp, rối loạn chức năng tim (bao gồm suy tim, suy thất trái cấp tính, rối loạn chức năng tâm trương và phì đại thất) xảy ra ở 1,7% bệnh nhân, bao gồm các phản ứng có hại độ 3 ở 1,1% bệnh nhân.
Trong INVICTUS, tỷ lệ tống máu giảm độ 3 xảy ra ở 1,3% trong số 77 bệnh nhân được điều trị Qinlock và những người có siêu âm tim cơ bản và ít nhất một lần siêu âm tim sau cơ sở. Trong nhóm dân số an toàn gộp lại, tỷ lệ tống máu giảm độ 3 xảy ra ở 1,9% trong số 263 bệnh nhân được điều trị Qinlock và những người có đường cơ bản và ít nhất một siêu âm tim sau đường cơ bản.
Ở INVICTUS, rối loạn chức năng tim dẫn đến ngừng liều ở 1,2% trong số 85 bệnh nhân được dùng Qinlock. Độ an toàn của Qinlock chưa được đánh giá ở những bệnh nhân có phân suất tống máu cơ bản dưới 50%. Đánh giá phân suất tống máu bằng siêu âm tim hoặc quét MUGA trước khi bắt đầu Qinlock và trong quá trình điều trị, theo chỉ định lâm sàng. Ngưng vĩnh viễn Qinlock đối với rối loạn chức năng tâm thu thất trái độ 3 hoặc 4.
Nguy cơ suy giảm khả năng chữa lành vết thương: Qinlock có khả năng ảnh hưởng xấu đến quá trình chữa lành vết thương. Giữ lại Qinlock ít nhất 1 tuần trước khi phẫu thuật tự chọn. Không dùng trong ít nhất 2 tuần sau khi phẫu thuật lớn và cho đến khi vết thương lành hẳn. Sự an toàn của việc tiếp tục Qinlock sau khi giải quyết các biến chứng chữa lành vết thương vẫn chưa được thiết lập.
Nhạy cảm với ánh sáng: Qinlock có thể gây ra phản ứng nhạy cảm với ánh sáng. Trong 621 bệnh nhân được điều trị bằng Qinlock trong các thử nghiệm lâm sàng, phản ứng nhạy cảm với ánh sáng xảy ra ở 0,6% bệnh nhân. Khuyên bệnh nhân hạn chế tiếp xúc trực tiếp với tia cực tím trong quá trình điều trị bằng Qinlock và ít nhất 1 tuần sau khi ngừng điều trị.
Độc tính phôi thai-thai nhi: Qinlock có thể gây hại cho thai nhi khi dùng cho phụ nữ mang thai. Tư vấn cho phụ nữ mang thai về nguy cơ tiềm ẩn đối với thai nhi. Tư vấn cho nữ giới có khả năng sinh sản và nam giới có bạn tình nữ có khả năng sinh sản nên sử dụng biện pháp tránh thai hiệu quả trong quá trình điều trị và trong 1 tuần sau liều cuối cùng. Do khả năng xảy ra các phản ứng phụ nghiêm trọng ở trẻ bú mẹ, khuyên phụ nữ không nên cho con bú trong quá trình điều trị và trong 1 tuần sau liều cuối cùng. Qinlock có thể làm suy giảm khả năng sinh sản ở con đực có khả năng sinh sản.
Phản ứng có hại: Các phản ứng có hại phổ biến nhất (≥20%) là rụng tóc, mệt mỏi, buồn nôn, đau bụng, táo bón, đau cơ, tiêu chảy, giảm cảm giác thèm ăn, PPES và nôn mửa. Các bất thường trong phòng thí nghiệm độ 3 hoặc 4 phổ biến nhất (≥4%) là tăng lipase và giảm phốt phát.
Tính an toàn và hiệu quả của Qinlock ở bệnh nhân nhi vẫn chưa được thiết lập.
Sử dụng thuốc ức chế CYP3A mạnh một cách thận trọng. Theo dõi bệnh nhân được sử dụng thuốc ức chế CYP3A mạnh thường xuyên hơn để phát hiện các phản ứng có hại. Tránh sử dụng đồng thời với các cảm ứng CYP3A mạnh và trung bình. Nếu không thể tránh khỏi thuốc cảm ứng CYP3A vừa phải, hãy tăng tần suất dùng Qinlock từ liều khuyến cáo 150 mg mỗi ngày một lần lên 150 mg hai lần mỗi ngày trong thời gian dùng đồng thời. Nếu ngưng dùng đồng thời thuốc cảm ứng CYP3A vừa phải, hãy tiếp tục liều Qinlock trở lại 150 mg mỗi ngày một lần trong 14 ngày sau khi ngưng dùng thuốc cảm ứng CYP3A vừa phải.
Thuốc Lucirip Ripretinib giá bao nhiêu?
Giá Thuốc Lucirip Ripretinib: Tư vấn 0778718459Thuốc Lucirip Ripretinib mua ở đâu?
Hà Nội: 80 Vũ Trọng Phụng, Thanh XuânHCM: 152 Lạc Long Quân, Phường 3, quận 11
Tài liệu tham khảo: Ripretinib: Uses, Interactions, Mechanism of Action | DrugBank
Mua ngay
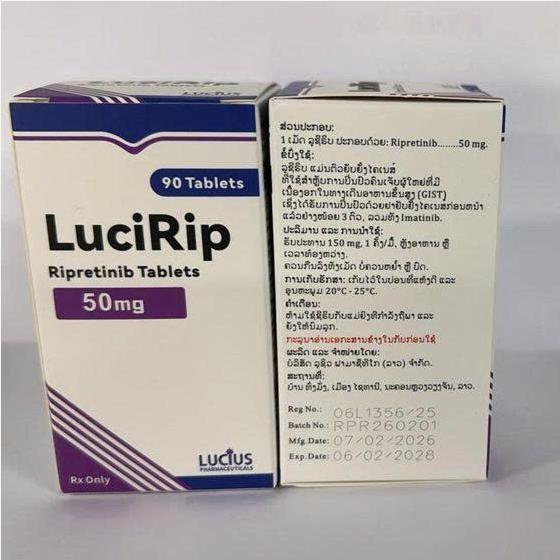
Thuốc Lucirip Ripretinib 50mg giá bao nhiêu
0đ
Số lượng: 1
THÔNG TIN KHÁCH HÀNG
ĐỊA CHỈ GIAO HÀNG
HÌNH THỨC THANH TOÁN
Thông tin vận chuyển
Hiện tại hệ thống nhận đơn hàng tự động của chúng tôi đang trong quá trình được hoàn thiện. Vì vậy khách hàng vui lòng liên hệ 0972945305 để đặt hàng và số 0906297798 để được tư vấn
THÔNG TIN ĐẶT HÀNG CỦA BẠN

Thuốc Lucirip Ripretinib 50mg giá bao nhiêu
0đ
Số lượng: 1
Tiền sản phẩm
THÔNG TIN KHÁCH HÀNG
- Họ và tên:
- Điện thoại:
- Email:
ĐỊA CHỈ GIAO HÀNG
- Địa chỉ:
- Quận / huyện:
- Tỉnh / thành phố:
- Phí vận chuyển:
- Ghi chú:
HÌNH THỨC THANH TOÁN